ПОМІРКУЙТЕ
По скільки орбіталей містять різні енергетичні рівні та по скільки електронів можуть максимально вміщувати енергетичні рівні: перший, другий, третій тощо?
Кількість орбіталей на енергетичному рівні обчислюється за формулою $n^2$, а максимальна кількість електронів — за формулою $2n^2$. Відповідно, перший рівень містить 1 орбіталь і максимально 2 електрони, другий — 4 орбіталі та 8 електронів, а третій — 9 орбіталей та 18 електронів.
Які електрони мають меншу енергію: ті, які перебувають на енергетичному рівні, ближчому до ядра, чи навпаки?
Меншу енергію мають ті електрони, які перебувають на енергетичному рівні, що розташований ближче до ядра атома.
Якщо другий енергетичний рівень може максимально вміщувати 8 електронів, то в якого хімічного елемента другий рівень заповниться повністю?
Другий енергетичний рівень повністю заповнюється в атомі хімічного елемента з порядковим номером 10 — Неону.
Як ви вважаєте, який рівень називають зовнішнім?
На мою думку, зовнішнім рівнем називають останній енергетичний рівень в атомі, на якому ще розташовані електрони.
Якою буде енергія електронів на зовнішньому енергетичному рівні порівняно з іншими електронами цього атома: найбільшою чи найменшою?
Енергія електронів на зовнішньому рівні буде найбільшою порівняно з енергією електронів на всіх інших рівнях цього атома.
Для електронних оболонок, моделі яких наведено вище в цьому параграфі, визначте число електронів на зовнішньому енергетичному рівні.
Згідно з наведеними у параграфі моделями, число електронів на зовнішньому рівні становить: у Гідрогену — 1, у Гелію — 2, у Літію — 1, у Берилію — 2, у Бору — 3, у Карбону — 4, у Неону — 8, у Натрію — 1, у Аргону — 8 та у Калію — 1.
ДОСЛІДЖУЄМО, МОДЕЛЮЄМО, ПРОЄКТУЄМО
Використовуючи підручні матеріали (дроти, намистини, канцелярські скріпки тощо), створіть статичну 2D- або 3D-модель атома (на вибір із перших 20 хімічних елементів) з урахуванням розподілу електронів по енергетичних рівнях.
На мою думку, найкращим варіантом для моделювання є атом Магнію (порядковий номер 12), який має три енергетичні рівні. Для створення 3D-моделі я використав пластилінове ядро в центрі та три концентричні кільця з дроту як енергетичні рівні: на першому (найближчому до ядра) я закріпив 2 намистини-електрони, на другому — 8 намистин, а на зовнішньому третьому рівні розмістив 2 намистини.
ПОМІРКУЙТЕ
Порівняйте максимальну місткість енергетичних рівнів і число хімічних елементів у кожному періоді.
Для першого та другого періодів максимальна місткість енергетичних рівнів (2 та 8 електронів відповідно) повністю збігається з кількістю хімічних елементів у цих періодах. Починаючи з третього періоду, кількість елементів стає меншою за максимальну місткість рівня: у третьому періоді 8 елементів при місткості рівня 18, а у четвертому періоді — 18 елементів при місткості рівня 32.
Порівняйте число електронів на зовнішньому енергетичному рівні атомів і номер групи Періодичної таблиці, у якій розміщено хімічний елемент.
Для елементів 1-ї та 2-ї груп число електронів на зовнішньому рівні точно дорівнює номеру групи, в якій вони розташовані. У хімічних елементів 13–18 груп кількість зовнішніх електронів відповідає номеру групи мінус десять (наприклад, елементи 17-ї групи мають 7 електронів на зовнішньому рівні).
РОЗУМІННЯ ЯВИЩ ПРИРОДИ (РОБОТА В ГРУПАХ)
322. Скільки електронів міститься на зовнішньому енергетичному рівні атомів: а) Гелію; б) Літію; в) Берилію; г) Бору; д) Карбону; е) Оксигену; є) Арсену; ж) Стануму; з) Барію?
На зовнішньому енергетичному рівні вказаних атомів міститься така кількість електронів: а) Гелію — 2; б) Літію — 1; в) Берилію — 2; г) Бору — 3; д) Карбону — 4; е) Оксигену — 6; є) Арсену — 5; ж) Стануму — 4; з) Барію — 2.
321. Скільки енергетичних рівнів зайнято електронами в атомах: а) Карбону, Силіцію, Германію; б) Берилію, Магнію, Кальцію; в) Флуору, Хлору, Йоду?
Число енергетичних рівнів в атомі відповідає номеру періоду, у якому розташований елемент: а) у Карбону — 2 рівні, у Силіцію — 3 рівні, у Германію — 4 рівні; б) у Берилію — 2 рівні, у Магнію — 3 рівні, у Кальцію — 4 рівні; в) у Флуору — 2 рівні, у Хлору — 3 рівні, у Йоду — 5 рівнів.
322. Назвіть два хімічні елементи, в атомах яких повністю заповнені зовнішні енергетичні рівні.
Повністю заповнені зовнішні енергетичні рівні мають інертні елементи, наприклад, Гелій та Неон.
323. Для хімічних елементів № 1–20 визначте: а) число електронних пар на зовнішньому енергетичному рівні; б) число неспарених електронів на зовнішньому енергетичному рівні.
- Гідроген (H): а) 0 пар; б) 1 неспарений електрон.
- Гелій (He): а) 1 пара; б) 0 неспарених електронів.
- Літій (Li): а) 0 пар; б) 1 неспарений електрон.
- Берилій (Be): а) 1 пара; б) 0 неспарених електронів.
- Бор (B): а) 1 пара; б) 1 неспарений електрон.
- Карбон (C): а) 1 пара; б) 2 неспарених електрони.
- Нітроген (N): а) 1 пара; б) 3 неспарених електрони.
- Оксиген (O): а) 2 пари; б) 2 неспарених електрони.
- Флуор (F): а) 3 пари; б) 1 неспарений електрон.
- Неон (Ne): а) 4 пари; б) 0 неспарених електронів.
- Натрій (Na): а) 0 пар; б) 1 неспарений електрон.
- Магній (Mg): а) 1 пара; б) 0 неспарених електронів.
- Алюміній (Al): а) 1 пара; б) 1 неспарений електрон.
- Силіцій (Si): а) 1 пара; б) 2 неспарених електрони.
- Фосфор (P): а) 1 пара; б) 3 неспарених електрони.
- Сульфур (S): а) 2 пари; б) 2 неспарених електрони.
- Хлор (Cl): а) 3 пари; б) 1 неспарений електрон.
- Аргон (Ar): а) 4 пари; б) 0 неспарених електронів.
- Калій (K): а) 0 пар; б) 1 неспарений електрон.
- Кальцій (Ca): а) 1 пара; б) 0 неспарених електронів.
324. Зобразіть будову електронних оболонок атомів Нітрогену та Фосфору. Що спільного в будові електронних оболонок цих атомів і чим вони відрізняються?
Схеми будови атомів:
Нітроген (N) +7 )2 )5

Фосфор (P) +15 )2 )8 )5
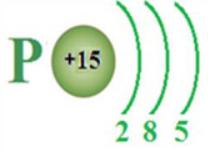
Спільним є те, що обидва атоми мають на зовнішньому енергетичному рівні по 5 електронів. Відрізняються вони загальною кількістю енергетичних рівнів: у Нітрогену їх два, а у Фосфору — три.
325. Які хімічні елементи є електронними аналогами Оксигену? Зобразіть будову електронної оболонки атома одного з них.
Електронними аналогами Оксигену є елементи головної підгрупи VI групи (16 групи): Сульфур (S), Селен (Se), Телур (Te) та Полоній (Po).
Схема будови електронної оболонки атома Сульфуру: +16 )2 )8 )6.

326. Порівняйте властивості хімічних елементів (металічний чи неметалічний) із числом електронів на зовнішньому рівні атомів. Сформулюйте гіпотезу щодо виявленої вами закономірності.
Металічні елементи мають на зовнішньому енергетичному рівні невелику кількість електронів (зазвичай від 1 до 3), тоді як у неметалічних елементів число зовнішніх електронів є більшим (від 4 до 8). На мою думку, можна висунути гіпотезу, що металічні або неметалічні властивості елемента залежать від кількості електронів на його зовнішньому рівні: чим менше електронів, тим легше атому їх віддавати, що характерно для металів, а велика кількість електронів зумовлює здатність атому приєднувати їх, що притаманно неметалам.
