ДОСЛІДЖУЄМО, МОДЕЛЮЄМО, ПРОЄКТУЄМО
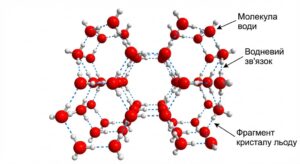
Використовуючи підручні матеріали (пластилін, намистини, дріт тощо), виготовте моделі молекул води та з’єднайте їх водневими зв’язками, створивши фрагмент кристалу льоду. За можливості створіть комп’ютерну 3D-модель.
ПОМІРКУЙТЕ
За малюнком 3.1 проаналізуйте вплив водневого зв’язку на температуру кипіння молекулярних речовин.
Наявність водневих зв’язків між молекулами води зумовлює її аномально високу температуру кипіння (100 °C) порівняно з іншими речовинами зі схожою молекулярною масою. Речовини, у яких водневий зв’язок відсутній, як-от сірководень ($H_2S$) або кисень ($O_2$), мають значно нижчі температури кипіння (–60,8 °C та –183 °C відповідно), попри більшу або близьку молекулярну масу. Це пояснюється необхідністю витрачання додаткової енергії на руйнування водневих зв’язків між молекулами під час переходу речовини з рідкого стану в газуватий.
ДОСЛІДЖУЄМО, МОДЕЛЮЄМО, ПРОЄКТУЄМО
Дослід 1. Акуратно наповніть до краю пробірку водою, щоб зовні пробірка залишилася сухою. Після цього акуратно піпеткою додавайте воду краплинами в пробірку. Що ви спостерігаєте? Чим це можна пояснити?
Під час додавання крапель вода не виливається з пробірки одразу, а утворює над її краями опуклу «гірку». Це явище пояснюється високим поверхневим натягом води, який виникає завдяки наявності водневих зв’язків, що міцно утримують молекули поверхневого шару разом, створюючи подібність до еластичної плівки.
Повторіть цей дослід, але замість чистої води використайте розчин мила (1 %) або іншого мийного засобу.
У разі використання мильного розчину вода виливається з пробірки значно швидше, а «гірка» майже не утворюється. Це відбувається тому, що поверхнево-активні речовини в милі послаблюють водневі зв’язки між молекулами води, що призводить до значного зниження поверхневого натягу рідини.
Дослід 2. Широку посудину заповніть водою наполовину. На фільтрувальний папір покладіть швейну голку й акуратно помістіть їх разом на поверхню води. Фільтрувальний папір згодом просочиться водою та потоне. А що відбувається з голкою? Чим це можна пояснити?
Після того як папір тоне, сталева голка залишається на поверхні води. Це пояснюється тим, що сила поверхневого натягу води, зумовлена водневими зв’язками, виявляється достатньою, щоб утримувати вагу голки на поверхневій «плівці», якщо її покласти горизонтально та обережно.
ДОСЛІДЖУЄМО, МОДЕЛЮЄМО, ПРОЄКТУЄМО
У цю ж посудину акуратно долийте розчин мийного засобу. Що відбувається з голкою? Сформулюйте гіпотезу, яка б пояснювала ваші спостереження.
Після додавання розчину мийного засобу голка втрачає підтримку на поверхні та тоне. Гіпотеза: молекули мийного засобу послаблюють сили притягання між молекулами води (водневі зв’язки), що призводить до різкого зниження поверхневого натягу, який утримував металевий предмет.
Широку пробірку наполовину заповніть водою. Другу таку саму пробірку наполовину заповніть етиловим спиртом. Нагрівайте ці дві пробірки в пальнику впродовж 30 секунд. Після нагрівання виміряйте температуру рідин у пробірках термометром. Яка речовина нагрілася сильніше? Який висновок про теплоємність рідин можна зробити? Підтвердьте свої висновки даними з довідника.
Сильніше нагріється етиловий спирт. Це дозволяє зробити висновок, що теплоємність води значно більша, ніж теплоємність спирту, оскільки вода потребує більше енергії для підвищення температури на ту саму кількість градусів. Згідно з довідковими даними, питома теплоємність води становить $4200 \text{ Дж} \cdot \text{кг}^{-1} \cdot \text{°C}^{-1}$, тоді як етилового спирту — лише $2400 \text{ Дж} \cdot \text{кг}^{-1} \cdot \text{°C}^{-1}$.
РОБОТА З ІНФОРМАЦІЄЮ
20. Порівняйте ковалентний і водневий зв’язки, склавши для них діаграми Венна.
| Ковалентний зв’язок | Спільне | Водневий зв’язок |
|---|---|---|
| Є внутрішньомолекулярним і утворюється спільними електронними парами | Мають електромагнітну природу | Переважно міжмолекулярний і базується на електростатичній взаємодії |
| Має високу енергію зв’язку | Впливають на фізичні та хімічні властивості речовин | Значно слабший за ковалентний і зумовлює аномальні властивості води |
21. Схарактеризуйте вплив водневого зв’язку на: а) розчинність речовин у воді; б) теплоємність речовин; в) поверхневий натяг води.
а) Водневий зв’язок сприяє розчиненню у воді речовин, молекули яких можуть утворювати такі зв’язки з молекулами розчинника (наприклад, спирти, глюкоза, аміак).
б) Він зумовлює аномально високу теплоємність речовин, бо значна частина отриманої теплоти витрачається на руйнування водневих зв’язків між молекулами, а не на збільшення їхньої кінетичної енергії.
в) Завдяки сильному взаємному притяганню молекул через водневі зв’язки, на поверхні води створюється міцна плівка, що забезпечує високий показник поверхневого натягу.
22. Порівняйте фізичні властивості речовин, зазначених на малюнку 3.1 (с. 25). Який факт свідчить про наявність водневого зв’язку між молекулами води?
Порівняння показує, що вода має найменшу відносну молекулярну масу ($M_r = 18$) серед представлених сполук, проте її температура кипіння ($+100 \text{ °C}$) є найвищою. Факт наявності водневого зв’язку підтверджується тим, що кисень ($M_r = 32$) та сірководень ($M_r = 34$), які мають більшу масу, за звичайних умов є газами з дуже низькими температурами кипіння, тоді як вода залишається рідиною через потребу в додатковій енергії для руйнування міжмолекулярних зв’язків.
РОЗУМІННЯ ЯВИЩ ПРИРОДИ (РОБОТА В ГРУПАХ)
23. Зобразіть (схематично) утворення водневого зв’язку між молекулами: а) води й амоніаку; б) води й гідроген фториду.
а) Утворення водневого зв’язку між молекулою води та молекулою амоніаку:
graph LR
subgraph "Молекула води"
H1(H) --- O(O)
O --- H2(H)
end
O -. "водневий зв'язок" .-> H3(H)
subgraph "Молекула амоніаку"
H3 --- N(N)
N --- H4(H)
N --- H5(H)
end
б) Утворення водневого зв’язку між молекулою води та молекулою гідроген фториду:
graph LR
subgraph "Молекула води"
H1(H) --- O(O)
O --- H2(H)
end
O -. "водневий зв'язок" .-> H3(H)
subgraph "Молекула гідроген фториду"
H3 --- F(F)
end
24. Поясніть, у який спосіб теплоємність води пом’якшує коливання температури на планеті.
Вода має аномально високу питому теплоємність завдяки необхідності витрачати значну кількість енергії на руйнування водневих зв’язків між її молекулами під час нагрівання. Світовий океан поглинає величезну кількість сонячного тепла вдень або влітку, майже не підвищуючи власну температуру, а вночі або взимку поступово віддає цю енергію в атмосферу. Цей механізм теплообміну діє як глобальний терморегулятор, що запобігає критичному перегріву або переохолодженню поверхні Землі.
25. Проаналізуйте графіки та схарактеризуйте вплив водневих зв’язків на фізичні властивості речовин. Поясніть, що спільного й відмінного між речовинами на кожному графіку. Зобразіть схеми утворення водневих зв’язків молекулами цих сполук (між собою та з молекулами води).
Аналіз графіків свідчить, що наявність водневих зв’язків призводить до аномального підвищення температури кипіння речовин.
| Характеристика | Гідриди галогенів (HF, HCl, HBr, HI) | Гідриди халькогенів ($H_2O, H_2S, H_2Se, H_2Te$) |
|---|---|---|
| Спільне | Представлені бінарні сполуки елементів однієї групи з Гідрогеном. Для більшості сполук температура кипіння лінійно зростає зі збільшенням молекулярної маси. | Представлені бінарні сполуки елементів однієї групи з Гідрогеном. Для більшості сполук температура кипіння лінійно зростає зі збільшенням молекулярної маси. |
| Відмінне | Гідроген фторид (HF) має аномально високу температуру кипіння, що не відповідає загальній тенденції групи. | Вода ($H_2O$) має аномально високу температуру кипіння, що значно перевищує показники важчих аналогів. |
| Причина | Між молекулами HF виникають міцні водневі зв’язки, на руйнування яких потрібна додаткова енергія. | Між молекулами $H_2O$ виникають численні водневі зв’язки (кожна молекула утворює до чотирьох зв’язків). |
Схеми утворення водневих зв’язків (на прикладі HF та $H_2O$):
- Між молекулами HF:
graph LR
F1(F) --- H1(H)
H1 -.-> F2(F)
F2 --- H2(H)
H2 -.-> F3(F)
- Між молекулами HF та води:
graph LR
F(F) --- H1(H)
H1 -.-> O(O)
O --- H2(H)
O --- H3(H)
- Між молекулами води ($H_2O \cdots H_2O$):
graph LR
O1(O) --- H1(H)
O1 --- H2(H)
O1 -.-> H3(H)
H3 --- O2(O)
O2 --- H4(H)
26. Відомо, що намоклий бавовняний або лляний одяг висихає довше, ніж шерсть або пір’я тварин. Як пояснити ці явища, зважаючи на водневий зв’язок?
Бавовняні та лляні волокна складаються з целюлози, молекули якої містять велику кількість гідроксильних груп (-OH). Ці групи утворюють численні та міцні водневі зв’язки з молекулами води, що призводить до сильного утримування вологи всередині тканини. Шерсть і пір’я складаються з білків (кератину) і часто вкриті гідрофобними жироподібними речовинами, які не здатні утворювати водневі зв’язки з водою, тому волога не проникає глибоко в структуру волокон і швидко випаровується або стікає.
27. Як ви вважаєте, чому краплини води на деяких листках та інших поверхнях набувають форми кулі? Чому краплі дощу «скочуються» з листя лотоса, проте затримуються на шкірі?
Краплини води набувають форми кулі завдяки поверхневому натягу, який виникає через прагнення молекул води утворити максимальну кількість водневих зв’язків одна з одною, що мінімізує площу поверхні рідини. Листя лотоса має специфічну мікроструктуру та восковий наліт, які є гідрофобними (відштовхують воду) і не дозволяють молекулам води утворювати водневі зв’язки з поверхнею листка, тому крапля зберігає форму кулі та легко скочується. Поверхня шкіри людини є більш гідрофільною через наявність білків і пір, що дозволяє воді частково змочувати її та утримуватися за допомогою слабких міжмолекулярних взаємодій.
