НАВЧАЛЬНЕ ДОСЛІДЖЕННЯ 3
Мета: визначити об’єм вуглекислого газу, що міститься в пляшці газованої води, шляхом вимірювання втрати маси після дегазації.
Завдання 1. Проведіть вимірювання та заповніть таблицю результатів дослідження.
| Параметр вимірювання | Значення |
|---|---|
| Маса закритої пляшки з газованою водою ($m_1$), г | 524,5 |
| Маса пляшки після повного видалення газу ($m_2$), г | 522,3 |
| Маса виділеного вуглекислого газу ($m_{CO_2} = m_1 – m_2$), г | 2,2 |
| Об’єм напою в пляшці, л | 0,5 |
Завдання 2. Обчисліть об’єм виділеного вуглекислого газу за нормальних умов.
Відомо:
- $m_{CO_2} = 2,2\text{ г}$
- $M_{CO_2} = 44\text{ г/моль}$
- $V_m = 22,4\text{ л/моль}$
Знайти:
- $V_{CO_2} – ?$
Розв’язання:
$n_{CO_2} = \dfrac{m}{M}$
$n_{CO_2} = \dfrac{2,2}{44} = 0,05\text{ моль}$
$V_{CO_2} = n \cdot V_m$
$V_{CO_2} = 0,05 \cdot 22,4 = 1,12\text{ л}$
Відповідь: 1,12 л.
Завдання 3. Сформулюйте висновки, заповнивши пропуски у реченнях.
Розчинність вуглекислого газу у воді залежить від зовнішніх умов: вона збільшується при підвищенні тиску та зменшується при підвищенні температури. У дослідженому напої об’єм розчиненого газу перевищує об’єм самої рідини, що свідчить про те, що газ у пляшці перебуває під тиском.
НАВЧАЛЬНЕ ДОСЛІДЖЕННЯ 4
Мета: виготовити пересичений розчин натрію етаноату (або цукру) та спостерігати процес його швидкої кристалізації.
Завдання 1. Опишіть етапи приготування пересиченого розчину за допомогою схеми.
graph TD
A[Приготування насиченого розчину при високій температурі] --> B[Фільтрування гарячого розчину від домішок]
B --> C[Повільне охолодження розчину до кімнатної температури]
C --> D[Отримання нестабільного пересиченого розчину]
D --> E[Внесення кристала солі або механічний вплив]
E --> F[Швидка кристалізація надлишкової речовини]
Завдання 2. Заповніть таблицю спостережень під час виконання дослідження.
| Етап дослідження | Спостереження | Стан системи |
|---|---|---|
| Розчинення солі при нагріванні | Речовина повністю розчиняється у невеликій кількості води. | Насичений гарячий розчин. |
| Охолодження розчину | Осад не утворюється, розчин залишається прозорим. | Пересичений нестабільний розчин. |
| Додавання маленького кристалика | Миттєве зростання кристалів по всьому об’єму, виділення теплоти. | Гетерогенна система: кристал + насичений розчин. |
Завдання 3. Сформулюйте висновок про властивості пересичених розчинів.
Пересичені розчини містять більше розчиненої речовини, ніж необхідно для насичення за даної температури. Такі системи є вкрай нестабільними і переходять у стійкий стан (насичений розчин та осад) внаслідок механічного впливу або потрапляння центрів кристалізації.
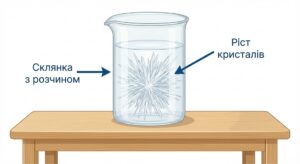
Завдання 4. Зобразіть вигляд кристалів, що утворюються під час кристалізації пересиченого розчину.