ДІЗНАЄТЕСЯ, ЗРОЗУМІЄТЕ, ВИКОРИСТАЄТЕ
Чому молекули певних речовин є полярними?
Полярні молекули утворюються з атомів із різною електронегативністю. Спільна електронна пара зсувається до атома, який сильніше притягує електрони. Через це на полюсах молекули з’являються часткові заряди: негативний ($ \delta- $) біля атома з більшою електронегативністю та позитивний ($ \delta+ $) біля атома з меншою.
Який вид хімічного зв’язку називають водневим зв’язком?
Водневий зв’язок — це електростатичне притягання між молекулами. Він виникає між атомами Гідрогену з частковим позитивним зарядом та атомами найбільш електронегативних елементів (Оксиген, Флуор, Нітроген), які мають вільні електронні пари й частковий негативний заряд.
Чому вода має аномальні фізичні властивості?
Аномальні властивості води зумовлені водневими зв’язками між її молекулами. Вони забезпечують вищі температури плавлення та кипіння, ніж у подібних за будовою сполук. Крім того, ці зв’язки створюють пухку кристалічну решітку льоду, тому його густина нижча за густину рідкої води.
Відшукайте в інтернеті температуру кипіння метану та порівняйте її з температурою кипіння води.
Метан ($CH_4$) кипить приблизно за $-161,5$ °C, а вода ($H_2O$) — за $+100$ °C. Хоча їхні відносні молекулярні маси дуже близькі ($M_r(CH_4) = 16$, $M_r(H_2O) = 18$), температура кипіння води вища на $261,5$ °C. Причина — наявність водневих зв’язків між молекулами води.
Спробуйте пояснити, чому між молекулами метану не утворюються водневі зв’язки, хоча ковалентний зв’язок С–Н є полярним. Скористайтеся моделлю молекули $CH_4$.
У метані немає водневих зв’язків, бо електронегативність Карбону занизька для створення значного позитивного заряду на атомах Гідрогену. До того ж молекула $CH_4$ має симетричну форму тетраедра. Полярність окремих зв’язків $C-H$ взаємно компенсується, тому молекула залишається неполярною.
ВИКОНАННЯ ЗАВДАНЬ ПАРАГРАФА
За даними таблиці побудуйте графік залежності температур плавлення цих сполук від значень їхніх відносних молекулярних мас і прокоментуйте його.
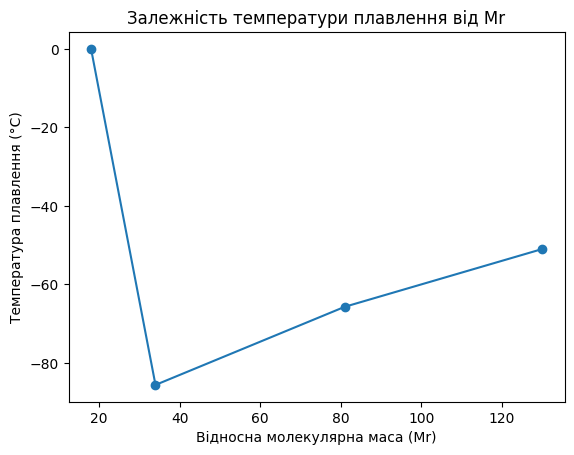
Про що свідчить цей графік?
Графік демонструє аномальні властивості води, які не залежать лише від молекулярної маси. Лід має вищу температуру плавлення, ніж сполуки Гідрогену з іншими елементами VI групи. Це підтверджує існування сильної міжмолекулярної взаємодії — водневого зв’язку.
ВИОКРЕМЛЮЄМО ОСНОВНЕ
Проаналізувавши матеріал, викладений у параграфі, запишіть у зошиті висновки про особливості будови молекули води, водневий зв’язок і його вплив на фізичні властивості води.
- Молекула води є полярною (диполем). Оксиген сильніше притягує електрони, а сама молекула має кутову форму.
- Між атомами Гідрогену однієї молекули та Оксигеном іншої формується водневий зв’язок.
- Саме він зумовлює аномально високі температури плавлення й кипіння.
- У льоді водневі зв’язки утримують молекули на відстані з утворенням порожнин, тому його густина нижча, ніж у рідкої води.
Сформулюйте цікаве запитання за темою параграфа і поставте його своїм однокласникам / однокласницям.
Чому водні організми виживають взимку, коли температура падає значно нижче нуля, а поверхня водойми замерзає?
Порівняйте свою і їхні відповіді та оцініть їх.
Правильна відповідь має пояснювати, що через водневі зв’язки густина льоду менша за густину води. Лід залишається на поверхні та діє як теплоізолятор. Він запобігає повному промерзанню водойми та рятує життя її мешканцям.
Поясніть, чому ваша оцінка саме така.
Оцінка залежить від того, чи встановлено логічний ланцюжок: від мікрорівня (водневий зв’язок) до макровластивостей (густина льоду) та їхньої ролі в природі.
ПЕРЕВІРМО СЕБЕ
374. Поясніть, чому молекула води є полярною.
Полярність води зумовлена вищою електронегативністю Оксигену, який відтягує на себе спільні електронні пари від Гідрогену. Через кутову форму молекули полюси зарядів не збігаються, утворюючи електричний диполь.
375. Прокоментуйте утворення водневого зв’язку у воді та льоді.
У рідкій воді через рух молекул водневі зв’язки безупинно виникають і рвуться. У твердому стані (льоді) вони фіксуються: кожна молекула стабільно зв’язана з чотирма сусідніми. Утворюється структура з порожнинами, тому лід легший за воду.
376. Іноді кажуть, що водневий зв’язок коректніше називати гідрогеновим зв’язком. На чому ґрунтується ця думка?
Сучасна хімічна номенклатура називає елемент $H$ Гідрогеном. Оскільки зв’язок формується саме за участю атомів цього елемента, назва «гідрогеновий зв’язок» є більш точною з наукового погляду.
ПОМІРКУЙМО
377. Зобразіть поряд графічні формули двох молекул амоніаку та позначте водневий зв’язок між цими частинками. Чому цей зв’язок є в рідкій і твердій речовині, але не утворюється в газуватому амоніаку?

(Три крапки показують притягання між атомом Гідрогену однієї молекули та вільною електронною парою Нітрогену іншої).
У рідкому й твердому станах молекули розташовані близько, тому виникає водневий зв’язок. У газах молекули рознесені далеко, а їхній швидкий рух розриває слабкі водневі зв’язки, не даючи утворитися стійким групам.
АНАЛІЗУЙМО
378. Графік, зображений на малюнку 93, свідчить про аномально високу температуру кипіння речовини HF порівняно з речовинами подібного складу і будови. Поясніть цей факт.
Висока температура кипіння флуороводню ($HF$) зумовлена водневими зв’язками. Флуор має найбільшу електронегативність, що робить зв’язок $H-F$ дуже полярним. Для розриву цієї сильної міжмолекулярної взаємодії при кипінні потрібно значно більше енергії порівняно з $HCl$, $HBr$ або $HI$.
У КОМАНДІ
379. За відомостями з інтернету з’ясуйте, яку температуру плавлення мав би лід, а яку температуру кипіння — вода в разі відсутності водневого зв’язку між молекулами. Який вигляд мала б тоді наша планета?
Без водневих зв’язків лід плавився б за температури близько $-100$ °C, а вода закипала б за $-80$ °C. Рідкої води на Землі просто не існувало б: усі океани стали б газом, а звичне для нас життя не змогло б з’явитися.
ФОРМУЙМО СЛОВНИЧОК
380. Випишіть ключові слова і словосполучення з тексту параграфа для укладання двомовного словничка.
- Водневий зв’язок — Hydrogen bond
- Полярність молекул — Molecular polarity
- Диполь — Dipole
- Електронегативність — Electronegativity
- Ковалентний полярний зв’язок — Polar covalent bond
- Електростатична взаємодія — Electrostatic interaction
ОЦІНЮЙМО СВОЇ ЗНАННЯ
381. Створіть у зошиті таблицю оцінювання ваших знань і заповніть її.
Зразок заповнення таблиці самооцінювання:
| Критерій знань | Рівень засвоєння (високий/середній/низький) |
|---|---|
| Розуміння природи водневого зв’язку | Високий |
| Пояснення аномальних властивостей води | Високий |
| Вміння графічно позначати водневий зв’язок | Середній |
| Розуміння впливу будови молекули на фізичні властивості | Високий |
