ДІЗНАЄТЕСЯ, ЗРОЗУМІЄТЕ, ВИКОРИСТАЄТЕ
Чому електронні оболонки атомів кількох хімічних елементів є найстійкішими?
Електронні оболонки інертних елементів найстійкіші через повністю заповнений зовнішній енергетичний рівень. Він містить вісім електронів (октет) або два, як у Гелію ($1s^2$).
Як однакові атоми сполучаються в молекули?
Атоми неметалів утворюють молекули завдяки зближенню та перекриванню електронних орбіталей, створюючи спільні електронні пари.
Який зв’язок між атомами називають простим, подвійним, потрійним?
Ковалентний зв’язок називають простим, якщо утворюється одна спільна пара електронів, подвійним — дві пари, потрійним — три пари.
Як складають електронні та графічні формули молекул?
В електронних формулах електрони зовнішнього рівня позначають крапками біля символу елемента. У графічних формулах спільну електронну пару зображують рискою.
Запишіть електронну формулу атома Гідрогену та зобразіть її графічний варіант.
Електронна формула Гідрогену — $1s^1$. Графічно її зображують однією квадратною коміркою (s-орбіталь) зі стрілкою вгору (неспарений електрон): 1s $$ \boxed{\uparrow} $$
Чому молекула водню складається з двох, а не більшої кількості атомів?
Кожен атом Гідрогену має один електрон на зовнішньому рівні й потребує ще одного для його завершення. Сполучення двох атомів створює спільну електронну пару. Це забезпечує обом атомам стійку двоелектронну оболонку, як у Гелію ($He$).
Чим відрізняється повна електронна формула молекули від спрощеної?
Повна електронна формула показує всі електрони зовнішніх рівнів (спільні та неподілені пари). Спрощена відображає лише спільні електронні пари, що утворюють хімічний зв’язок.
Складіть електронну формулу атома Нітрогену і зобразіть її графічний варіант. Cкільки неспарених електронів у цьому атомі?
Електронна формула Нітрогену — $1s^2 2s^2 2p^3$. Графічний варіант зовнішнього рівня:

Атом має три неспарені електрони на $2p$-підрівні.
Складіть повну електронну формулу молекули азоту.
Повна електронна формула азоту ($N_2$):
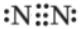
Три пари крапок між символами — це потрійний зв’язок (спільні пари). Крапки з боків — неподілені електронні пари кожного атома Нітрогену.
ВИОКРЕМЛЮЄМО ОСНОВНЕ
Проаналізувавши матеріал, викладений у параграфі, запишіть у зошиті висновки про те, електронні оболонки якого складу забезпечують стійкість атомів і як сполучені атоми в молекулах неметалів.
Найстійкіші електронні оболонки мають вісім електронів (октет), для першого періоду — два. Атоми неметалів утворюють ковалентний зв’язок через об’єднання неспарених електронів у спільні пари.
Сформулюйте цікаве запитання за темою параграфа і поставте його своїм однокласникам / однокласницям. Порівняйте свою і їхні відповіді та оцініть їх. Поясніть, чому ваша оцінка саме така.
Запитання: «Чому атоми Гідрогену утворюють молекулу $H_2$, а атоми Гелію залишаються поодинці?»
Відповідь: Гідроген має незавершену оболонку ($1s^1$) і прагне її добудувати. Гелій має стійку завершену оболонку ($1s^2$), тому зв’язків не утворює.
Оцінка: Пояснення ґрунтується на електронній будові атомів, що визначає хімічну активність елементів.
ВАШІ ДОСЯГНЕННЯ І ВІДКРИТТЯ
327. Який зв’язок називають ковалентним? Яка особливість електронної будови атомів, між якими утворюється цей зв’язок?
Ковалентний зв’язок утворюється за допомогою спільних електронних пар. Атоми для цього використовують неспарені електрони зовнішнього рівня, щоб досягти стійкого двоелектронного або восьмиелектронного стану.
328. Охарактеризуйте зв’язок у молекулі $Cl_2$. Назвіть орбіталі атомів Хлору, які зазнають перекривання.
Зв’язок у молекулі $Cl_2$ — ковалентний простий (одна спільна електронна пара). Відбувається перекривання $3p$-орбіталей атомів Хлору з неспареними електронами.
329. З якою кількістю атомів сполучений кожний атом у молекулі білого фосфору? Простими, подвійними чи потрійними є ковалентні зв’язки між атомами в молекулі $P_4$?
У тетраедричній молекулі $P_4$ кожен атом Фосфору сполучений із трьома іншими. Ковалентні зв’язки між ними — прості.
ВИКОНАЙМО ВПРАВУ
330. Складіть повну і спрощену електронні формули молекули $F_2$ та зобразіть графічну формулу цієї молекули.

ПОМІРКУЙМО
331. У молекулі кисню чи в молекулі азоту зв’язок між атомами, на вашу думку, має бути міцнішим? Правильність відповіді перевірте, відшукавши в інтернеті відомості про умови, за яких кожна молекула розпадається на атоми.
Зв’язок у молекулі азоту ($N_2$) міцніший через потрійний ковалентний зв’язок ($N \equiv N$). У молекулі кисню ($O_2$) він подвійний ($O = O$). Практика підтверджує: азот розпадається за температур понад $3000^\circ\text{C}$, кисень дисоціює значно легше.
СТВОРЮЙМО
Зобразіть графічну формулу молекули $S_8$, якщо кожний атом у ній сполучений з двома іншими простими ковалентними зв’язками.
Графічна формула $S_8$ — замкнене кільце у формі «корони», де вісім атомів Сульфуру з’єднані одинарними зв’язками:

ФОРМУЙМО СЛОВНИЧОК
Випишіть ключові слова і словосполучення з тексту параграфа для укладання двомовного словничка.
- Ковалентний зв’язок — covalent bond
- Спільна електронна пара — shared electron pair
- Електронна формула — electron formula
- Графічна (структурна) формула — graphic (structural) formula
- Простий (одинарний) зв’язок — single bond
- Подвійний зв’язок — double bond
- Потрійний зв’язок — triple bond
- Електронний октет — electron octet
- Неспарені електрони — unpaired electrons
- Інертні елементи — inert elements
ОЦІНЮЙМО СВОЇ ЗНАННЯ
Створіть у зошиті таблицю оцінювання ваших знань і заповніть її.
| Знання та вміння | Оцінка |
|---|---|
| Розумію механізм утворення ковалентного зв’язку | Засвоєно |
| Вмію складати електронні формули молекул | Засвоєно |
| Розрізняю типи ковалентних зв’язків за кратністю (простий, подвійний, потрійний) | Засвоєно |
| Вмію будувати графічні формули молекул простих речовин | Потребує практики |
| Розумію причину хімічної пасивності інертних газів | Засвоєно |
