ДІЗНАЄТЕСЯ, ЗРОЗУМІЄТЕ, ВИКОРИСТАЄТЕ
Чому розміщення електронів в атомі не безладне, а впорядковане?
Електрони розташовуються за принципом мінімальної енергії. Вони послідовно заповнюють енергетичні рівні та підрівні від найменшої енергії до найбільшої. Це забезпечує максимальну стійкість атома.
Як заповнювати енергетичні рівні та підрівні електронами в атомах хімічних елементів і складати електронні формули атомів?
Заповнення починається з першого рівня, найближчого до ядра, де енергія мінімальна. Формулу записують так: номер рівня, літера підрівня ($s, p, d, f$) та кількість електронів як верхній індекс (наприклад, $1s^2$). За принципом Паулі, одна орбіталь вміщує максимум два електрони з протилежними спінами.
Як класифікують хімічні елементи за електронною будовою атомів?
Елементи поділяють на $s$-, $p$-, $d$- та $f$-елементи. Це залежить від того, яка орбіталь останньою заповнюється електронами з найвищою енергією.
Узявши до уваги, що кожний електрон намагається зайняти вільну орбіталь підрівня, а в разі її відсутності «підселяється» в орбіталь до іншого електрона, складіть електронні формули атомів Нітрогену, Оксигену, Флуору та Неону, а також зобразіть графічні варіанти цих формул.
Нітроген ($N$): $1s^2 2s^2 2p^3$
Графічна формула:

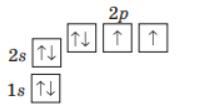
Оксиген ($O$): $1s^2 2s^2 2p^4$
Графічна формула:
Флуор ($F$): $1s^2 2s^2 2p^5$
Графічна формула:

Неон ($Ne$): $1s^2 2s^2 2p^6$
Графічна формула:

Запропонуйте гіпотезу щодо того, чому розміри атомів хімічних елементів у періоді зменшуються, а не збільшуються.
У періоді зліва направо заряд ядра зростає. Кількість енергетичних рівнів не змінюється, але ядро сильніше притягує зовнішні електрони. Тому радіус атома зменшується.
Складіть електронні формули атомів решти хімічних елементів 3-го періоду.
Електронні формули елементів 3-го періоду (від Магнію до Аргону):
- Магній ($_{12}Mg$): $1s^2 2s^2 2p^6 3s^2$
- Алюміній ($_{13}Al$): $1s^2 2s^2 2p^6 3s^2 3p^1$
- Силіцій ($_{14}Si$): $1s^2 2s^2 2p^6 3s^2 3p^2$
- Фосфор ($_{15}P$): $1s^2 2s^2 2p^6 3s^2 3p^3$
- Сульфур ($_{16}S$): $1s^2 2s^2 2p^6 3s^2 3p^4$
- Хлор ($_{17}Cl$): $1s^2 2s^2 2p^6 3s^2 3p^5$
- Аргон ($_{18}Ar$): $1s^2 2s^2 2p^6 3s^2 3p^6$
Запишіть електронну формулу атома елемента № 20 Кальцію.
Формула атома Кальцію ($Ca$): $1s^2 2s^2 2p^6 3s^2 3p^6 4s^2$.
До s- чи p-елементів належать Сульфур, Барій, Калій, Неон, Йод?
- $s$-елементи: Барій ($Ba$), Калій ($K$).
- $p$-елементи: Сульфур ($S$), Неон ($Ne$), Йод ($I$).
Назвіть неметалічні елементи 1—2-го періодів, які є винятками (щодо кількості зовнішніх електронів).
До винятків серед неметалів належать Гідроген ($H$, 1 електрон), Гелій ($He$, 2 електрони) та Бор ($B$, 3 електрони). Вони мають менше чотирьох електронів на зовнішньому рівні, що нетипово для неметалічних елементів.
ВИОКРЕМЛЮЄМО ОСНОВНЕ
Проаналізувавши матеріал, викладений у параграфі, запишіть у зошиті висновки про особливості електронної будови атомів хімічних елементів № 1—20 і послідовність заповнення електронами орбіталей у цих атомах.
Висновки щодо електронної будови атомів № 1—20:
- Електрони заповнюють орбіталі за принципом мінімальної енергії: $1s \rightarrow 2s \rightarrow 2p \rightarrow 3s \rightarrow 3p \rightarrow 4s$.
- Кількість енергетичних рівнів відповідає номеру періоду елемента.
- Кількість електронів на зовнішньому рівні в елементах головних підгруп дорівнює номеру групи (крім Гелію).
- Одна орбіталь містить максимум два електрони з протилежними спінами. На $p$-підрівні електрони спочатку розташовуються по одному у вільних орбіталях (правило Гунда).
- За останньою заповненою орбіталлю елементи поділяють на $s$- та $p$-елементи.
Сформулюйте цікаве запитання за темою параграфа і поставте його своїм однокласникам / однокласницям. Порівняйте свою і їхні відповіді та оцініть їх. Поясніть, чому ваша оцінка саме така.
Запитання: «Чому електрони в атомі Карбону на другому енергетичному рівні займають різні $p$-орбіталі, а не спаровуються в одній?»
Правильна відповідь: Електрони мають однаковий негативний заряд і відштовхуються. Розташування на різних орбіталях одного підрівня віддаляє їх. Це знижує енергію атома та підвищує його стійкість (правило Гунда).
ПЕРЕВІРМО СЕБЕ
309. Назвіть хімічний елемент, атом якого має таку електронну формулу: а) $1s^2 2s^2 2p^6 3s^2 3p^2$; б) $[He]2s^2 2p^5$; в) $[Ar]4s^2$.
- а) Силіцій ($Si$, протонне число 14).
- б) Флуор ($F$, протонне число 9).
- в) Кальцій ($Ca$, протонне число 20).
310. Атом на другому енергетичному рівні має 6 електронів. Скільки серед них спарених, а скільки — неспарених?
Конфігурація другого рівня — $2s^2 2p^4$. Графічний розподіл: $2s$ [⇅], $2p$ [⇅][↑][↑]. Серед шести електронів є чотири спарені (дві пари) і два неспарені.
311. Атоми яких елементів 2-го періоду мають один неспарений електрон, два неспарені електрони?
- Один неспарений електрон: Літій ($Li$, $2s^1$), Бор ($B$, $2p^1$), Флуор ($F$, $2p^5$).
- Два неспарені електрони: Карбон ($C$, $2p^2$), Оксиген ($O$, $2p^4$).
312. Укажіть хімічний елемент, електронну будову атома якого описує така графічна формула (варіанти а, б).
а) Електронна конфігурація: $1s^2 2s^2 2p^6 3s^2 3p^1$. Загальна кількість електронів: 13. Це Алюміній ($Al$).
б) Електронна конфігурація: $1s^2 2s^2 2p^6 3s^2 3p^4$. Загальна кількість електронів: 16. Це Сульфур ($S$).
АНАЛІЗУЙМО
313. Укажіть помилки в електронних формулах атомів: а) $1s^2 2s^3 2p^1$; б) $[Ar]3s^2 3p^2$; в) $1s^2 2s^2 2p^6 3s^1 3p^4$.
- а) $s$-орбіталь вміщує максимум два електрони. Правильний запис: $2s^2$.
- б) Аргон завершує 3-й період ($3s^2 3p^6$). Використання $[Ar]$ тут неможливе. Для Силіцію правильний запис: $[Ne]3s^2 3p^2$.
- в) Підрівень $3s$ має бути заповнений повністю ($3s^2$) перед початком заповнення $3p$. Правильно: $…3s^2 3p^3$.
У КОМАНДІ
314. Скориставшись періодичною таблицею, з’ясуйте: а) яких елементів більше — p-елементів чи d-елементів; б) які елементи — металічні чи неметалічні — переважають серед s-елементів, p-елементів.
- а) $d$-елементів більше (40), ніж $p$-елементів (36).
- б) Серед $s$-елементів переважають метали. Серед $p$-елементів більшість становлять неметали.
ПОМІРКУЙМО
315. Назвіть два елементи, в атомах яких кількість електронів у всіх s-орбіталях така сама, що й у р-орбіталях.
- Оксиген ($O$): $1s^2 2s^2 2p^4$ (4 $s$-електрони та 4 $p$-електрони).
- Магній ($Mg$): $1s^2 2s^2 2p^6 3s^2$ (6 $s$-електронів та 6 $p$-електронів).
ФОРМУЙМО СЛОВНИЧОК
316. Випишіть ключові слова і словосполучення з тексту параграфа для укладання двомовного словничка.
- Електронна будова атома — electronic structure of an atom
- Енергетичний рівень — energy level
- Підрівень — sublevel
- $s$-орбіталь — s-orbital
- $p$-орбіталь — p-orbital
- Електронна формула (конфігурація) — electron configuration
- Принцип мінімальної енергії — minimum energy principle
- Зовнішні електрони — outer (valence) electrons
ОЦІНЮЙМО СВОЇ ЗНАННЯ
317. Створіть у зошиті таблицю оцінювання ваших знань і заповніть її.
Приклад таблиці самооцінювання:
| Критерій оцінювання | Рівень знань (Низький/Середній/Високий) |
|---|---|
| Розуміння принципу мінімальної енергії | Високий |
| Вміння складати повні та скорочені електронні формули | Високий |
| Класифікація елементів за типом орбіталей ($s, p, d, f$) | Середній |
| Вміння визначати кількість зовнішніх електронів | Високий |
| Розуміння графічних електронних формул | Високий |
